《药品技术转让注册管理规定》解读 技术转让的核心要点与流程

药品技术转让是药品上市许可持有人制度下的关键环节,对于优化资源配置、促进产业升级具有重要意义。国家药品监督管理局颁布的《药品技术转让注册管理规定》(以下简称《规定》)为这一活动提供了明确的法规框架和操作指南。
一、 技术转让的定义与范畴
《规定》明确,药品技术转让是指药品技术的所有者按照本规定的要求,将药品生产技术转让给受让方药品生产企业,并由受让方药品生产企业申请药品注册的过程。这里的技术主要指药品的处方、生产工艺、质量标准、质量控制方法以及相关的技术资料和知识产权。转让范围通常包括新药技术转让和已有国家药品标准的药品技术转让。
二、 转让双方的基本条件
- 转让方(持有药品批准证明文件者)应具备对转让技术的合法所有权或处分权,且该药品批准文号必须有效。
- 受让方(药品生产企业)必须持有与转让药品剂型相一致的《药品生产许可证》和《药品生产质量管理规范》(GMP)认证证书,并具备相应的生产条件、检验能力和质量保证体系。
三、 技术转让注册的核心程序
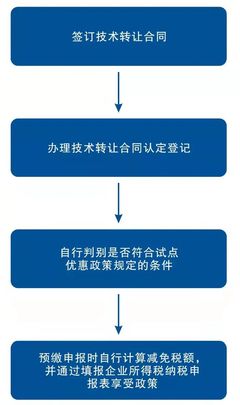
技术转让的注册申请,本质上是受让方就转让药品申请新的药品批准证明文件的过程。主要程序包括:
- 申请与受理:受让方向所在地省级药品监督管理部门提交技术转让注册申请及相关资料。
- 现场核查与抽样检验:药品监督管理部门对受让方的生产条件和试制现场进行核查,并对连续生产的3批样品进行抽样,送药品检验机构检验。
- 技术审评:国家药品监督管理局药品审评中心基于申报资料、现场核查报告和样品检验结果,对技术转让的可行性、受让方产品质量的可控性与一致性进行科学审评。
- 审批与发证:审评通过后,由国家药监局审批,符合规定的,发给新的药品批准文号,并注销转让方的原药品批准文号。
四、 申报资料的关键要求
申报资料是审评的核心依据,必须全面、真实、规范。重点包括:
- 证明转让合法性的协议或合同。
- 转让药品的批准证明文件复印件。
- 详细的工艺验证资料和质量对比研究资料,证明受让方产品与原产品在质量、安全性和有效性上保持一致。
- 受让方相关的资质证明文件(生产许可证、GMP证书等)。
五、 风险控制与监管重点
《规定》着重强调了技术转让过程中的质量风险控制。监管的核心在于确保技术转移后,受让方生产的产品质量与转让方原产品“等同”,不能因生产场地、设备、工艺参数的转移而产生质量差异。因此,工艺验证、持续稳定性考察以及严格的质量对比研究是成功通过技术审评的基石。
《药品技术转让注册管理规定》的出台,规范了药品技术转让行为,保障了技术转让过程中药品质量的延续性和可控性。深入理解《规定》要求,扎实做好工艺验证和质量研究,是顺利完成技术转让、实现技术价值转化的关键。这不仅是法规合规的要求,更是对公众用药安全负责的体现。
如若转载,请注明出处:http://www.xdzbjqq.com/product/76.html
更新时间:2026-06-03 21:58:40